Biothérapies et thérapies ciblées
Les traitements de fond se distinguent des traitements dits " symptomatiques " (antalgiques, anti-inflammatoires, etc.). Leur utilisation a pour objectif de contrôler la maladie inflammatoire sur le long terme tout en réduisant la consommation des traitements symptomatiques. Dans la nomenclature anglo-saxonne, qui tend à s'imposer, nous parlons de DMARD (Disease-Modifying AntiRheumatic Drugs) pour désigner ces traitements de fond.
On distingue deux classes de traitements de fond ou DMARD, conventionnels et ciblés :
![]() Parmi les bDMARD, on distingue les originaux (boDMARD) et les biosimilaires (bsDMARD), qui sont sur le marché français depuis 2016. Les biosimilaires correspondent à des copies des molécules originales mais qui doivent démontrer une efficacité et une tolérance similaires à la molécule originale dans un essai clinique randomisé en double aveugle dans au moins une des pathologies pour laquelle la molécule originale a une indication. Leur coût est moins élevé et pourrait permettre d'envisager des économies.
Parmi les bDMARD, on distingue les originaux (boDMARD) et les biosimilaires (bsDMARD), qui sont sur le marché français depuis 2016. Les biosimilaires correspondent à des copies des molécules originales mais qui doivent démontrer une efficacité et une tolérance similaires à la molécule originale dans un essai clinique randomisé en double aveugle dans au moins une des pathologies pour laquelle la molécule originale a une indication. Leur coût est moins élevé et pourrait permettre d'envisager des économies.
![]() Il existe actuellement deux principaux modes d'action des biomédicaments utilisés en rhumatologie (fig. 22.1).
Il existe actuellement deux principaux modes d'action des biomédicaments utilisés en rhumatologie (fig. 22.1).
Fig. 22.1. ![]() Mécanismes d'action des différents biomédicaments (bDMARD).
Mécanismes d'action des différents biomédicaments (bDMARD).
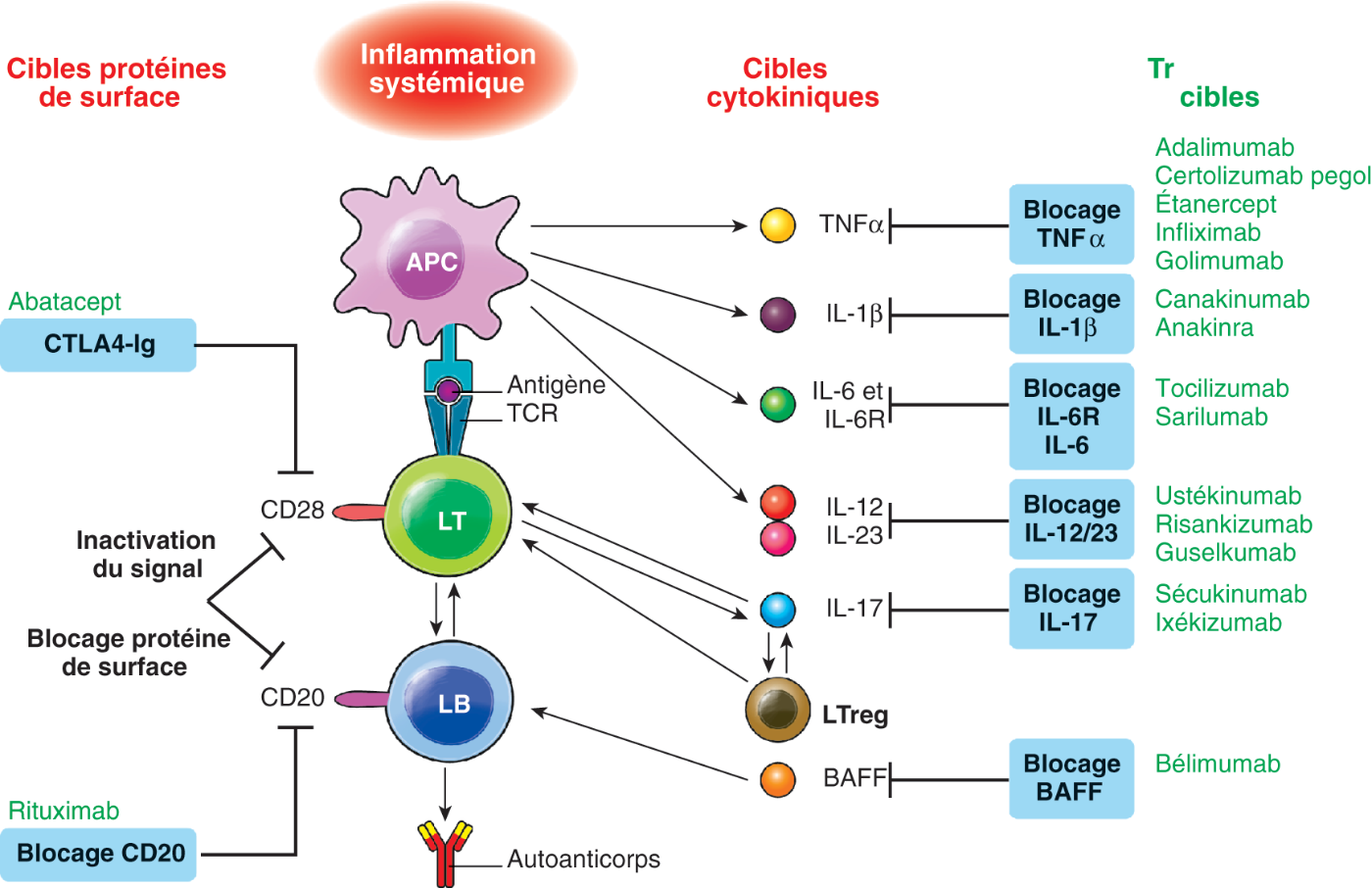
Les cibles des différents biomédicaments sont précisées avec soit neutralisation d'une cytokine soit interaction avec une molécule située à la surface d'une cellule.
CPA : cellule présentatrice d'antigènes ; LT : lymphocyte T ; LB : lymphocyte B. CTLA4 : Cytotoxic T-Lymphocyte-Associated protein 4 ; IL : interleukine ; TNF : Tumor Necrosis factor ; TCR : T cell receptor ; BAFF : B cell Activated Factor ; CD : Cluster of Differenciation.
Adapté de : Morel, et al. Médecine/sciences 2019;35:1029-33.
Le premier mode d'action consiste à neutraliser directement une cytokine impliquée dans l'immunité (par exemple, TNF, IL-17, IL-23, IL-1) ou bloquer le récepteur sur lequel se lie la cytokine (par exemple, récepteurs de l'IL-6, de l'IL-1, de l'IL-12).
Le deuxième mode d'action consiste à cibler une molécule membranaire spécifique d'une cellule qui peut :
Un biomédicament peut se faire :
![]() Concernant la nomenclature de la DCI d'un biomédicament, si le suffixe indique donc le mécanisme d'action (anticorps monoclonal ou protéine de fusion), le préfixe indique l'origine de la molécule (o-, xi-, zu-, mu- pour des origines respectivement murine, chimérique, humanisée ou humaine) avec pour corollaire un risque plus ou moins élevé d'immunogénicité de celle-ci.
Concernant la nomenclature de la DCI d'un biomédicament, si le suffixe indique donc le mécanisme d'action (anticorps monoclonal ou protéine de fusion), le préfixe indique l'origine de la molécule (o-, xi-, zu-, mu- pour des origines respectivement murine, chimérique, humanisée ou humaine) avec pour corollaire un risque plus ou moins élevé d'immunogénicité de celle-ci.
L'antépénultième syllabe indique quant à elle le registre thérapeutique pour lequel était initialement destinée la molécule tels que " tu " pour tumeur, " vi " pour virus, " li " ou " ki " pour le système immunitaire...
![]() Les inhibiteurs de kinases sont de petites protéines de synthèse chimique capables de neutraliser l'activation des tyrosine kinases comme JAK (fig. 22.2). Il existe quatre isotypes différents de JAK : JAK1, JAK2, JAK3 et Tyk2. Les JAK sont activées après la liaison entre la cytokine (par exemple, l'IL-6) et son récepteur (IL-6R) et induisent une phosphorylation du facteur de transcription STAT qui peut, sous cette forme phosphorylée, franchir l'enveloppe nucléaire et se fixer sur les gènes codant des protéines de l'inflammation.
Les inhibiteurs de kinases sont de petites protéines de synthèse chimique capables de neutraliser l'activation des tyrosine kinases comme JAK (fig. 22.2). Il existe quatre isotypes différents de JAK : JAK1, JAK2, JAK3 et Tyk2. Les JAK sont activées après la liaison entre la cytokine (par exemple, l'IL-6) et son récepteur (IL-6R) et induisent une phosphorylation du facteur de transcription STAT qui peut, sous cette forme phosphorylée, franchir l'enveloppe nucléaire et se fixer sur les gènes codant des protéines de l'inflammation.
Fig. 22.2. ![]() Mécanisme d'action des JAKi : exemple de la voie de signalisation de l'IL-6.
Mécanisme d'action des JAKi : exemple de la voie de signalisation de l'IL-6.
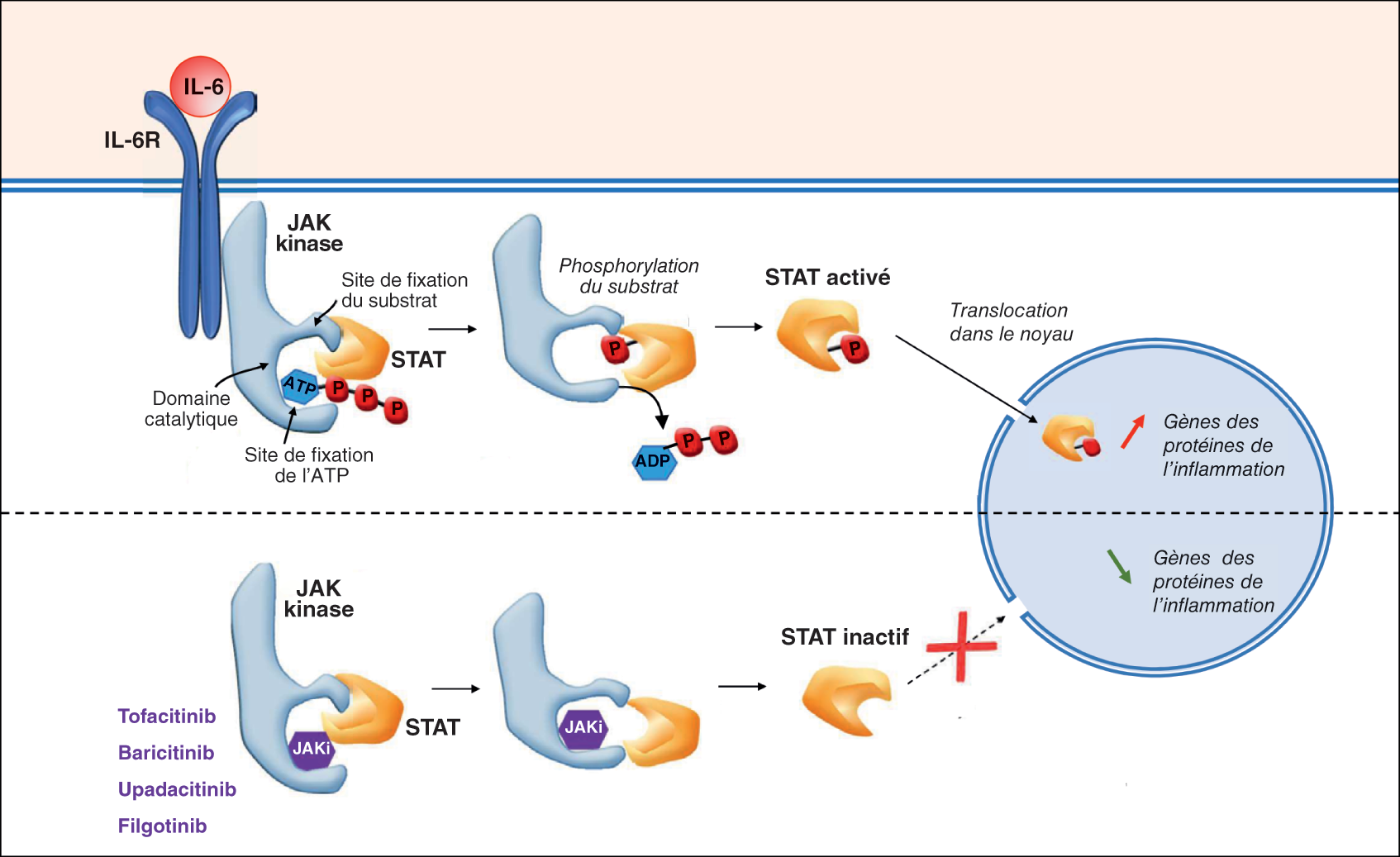
Le JAKi s'insère dans le domaine catalytique de la kinase JAK à la place de l'ATP et empêche ainsi la phosphorylation du facteur de transcription STAT. Le facteur de transcription STAT doit être phosphorylé pour entrer dans le noyau et activer la synthèse de protéines de l'inflammation.
JAK : Janus kinase ; STAT : Signal Transducers and Activators of Transcription ; ATP : adénosine triphosphate ; ADP : adénosine diphosphate.
Adapté de : Sweeney SE, et al. Nat Clin Pract Rheumatol 2007;3:651-60. Illustration de Carole Fumat.
Nous disposons actuellement en France dans le domaine de la rhumatologie de :
cinq anti-TNF : ![]() infliximab, étanercept, adalimumab, certolizumab, golimumab ;
infliximab, étanercept, adalimumab, certolizumab, golimumab ;
![]() un anti-lymphocyte B CD20 :
un anti-lymphocyte B CD20 : ![]() rituximab ;
rituximab ;
![]() un inhibiteur de la différenciation et de l'activation des lymphocytes B :
un inhibiteur de la différenciation et de l'activation des lymphocytes B : ![]() bélimumab ;
bélimumab ;
![]() un inhibiteur de la co-activation des lymphocytes T :
un inhibiteur de la co-activation des lymphocytes T : ![]() abatacept ;
abatacept ;
![]() deux anticorps anti-récepteur de l'IL-6 :
deux anticorps anti-récepteur de l'IL-6 : ![]() tocilizumab, sarilumab ;
tocilizumab, sarilumab ;
![]() un récepteur antagoniste de l'IL-1 :
un récepteur antagoniste de l'IL-1 : ![]() anakinra ;
anakinra ;
![]() un anticorps anti-IL-1 :
un anticorps anti-IL-1 : ![]() canakinumab ;
canakinumab ;
![]() des anticorps anti-IL-17 :
des anticorps anti-IL-17 : ![]() sécukinumab, ixékizumab, bimékizumab ;
sécukinumab, ixékizumab, bimékizumab ;
![]() des anticorps anti-IL-23 :
des anticorps anti-IL-23 : ![]() guselkumab, rizankizumab ;
guselkumab, rizankizumab ;
![]() un anticorps anti-IL-12/IL-23 :
un anticorps anti-IL-12/IL-23 : ![]() ustékinumab ;
ustékinumab ;
![]() un anticorps anti-RANKL :
un anticorps anti-RANKL : ![]() dénosumab, dans l'ostéoporose ;
dénosumab, dans l'ostéoporose ;
![]() des inhibiteurs des kinases JAK :
des inhibiteurs des kinases JAK : ![]() tofacitinib, baricitinib, upadacitinib, filgotinib ;
tofacitinib, baricitinib, upadacitinib, filgotinib ;
![]() un inhibiteur de la phosphodiestérase de type 4 :
un inhibiteur de la phosphodiestérase de type 4 : ![]() aprémilast ;
aprémilast ;
![]() plusieurs biosimilaires commercialisés en France depuis 2016
plusieurs biosimilaires commercialisés en France depuis 2016 ![]() pour l'infliximab, l'étanercept, l'adalimumab, le rituximab et le tocilizumab.
pour l'infliximab, l'étanercept, l'adalimumab, le rituximab et le tocilizumab.
![]() Chaque thérapeutique ciblée a des indications spécifiques et toutes ne sont pas efficaces sur les mêmes pathologies.
Chaque thérapeutique ciblée a des indications spécifiques et toutes ne sont pas efficaces sur les mêmes pathologies.
Par exemple, si les anti-TNFa fonctionnent à la fois dans la polyarthrite rhumatoïde et les spondyloarthrites, les anti-IL-6R fonctionnent dans la PR et non dans les spondyloarthrites, et les anti-IL-17 ont un effet dans les spondyloarthrites mais pas dans la PR :
la stratégie thérapeutique dans la polyarthrite rhumatoïde (cf. fig. 17.10 au chapitre 17) débute par la prescription de csDMARD (méthotrexate et si contre-indication, léflunomide) ; ce n'est qu'en cas d'échec des csDMARD incluant au moins le méthotrexate que l'on a recours à un traitement ciblé ;
dans les spondyloarthrites axiales, périphériques articulaires, périphériques enthésitiques (cf. fig. 18.10 au chapitre 18), un traitement ciblé peut être envisagé en cas de rhumatisme inflammatoire non contrôlé malgré les AINS dans les formes axiales et les traitements de fond conventionnels (csDMARD) dans les formes périphériques.
![]() La prescription des biomédicaments (à l'exception du dénosumab) et de JAKi est du ressort du médecin spécialiste de la pathologie concernée. Cette prescription est actuellement encadrée par une prescription initiale hospitalière (PIH). Les biomédicaments et JAKi ne peuvent donc être initiés que par certaines spécialités et certains spécialistes exerçant dans une structure hospitalière ou clinique, mais ils peuvent être renouvelés par les médecins spécialistes libéraux. La PIH devrait être levée en 2024 pour les biomédicaments.
La prescription des biomédicaments (à l'exception du dénosumab) et de JAKi est du ressort du médecin spécialiste de la pathologie concernée. Cette prescription est actuellement encadrée par une prescription initiale hospitalière (PIH). Les biomédicaments et JAKi ne peuvent donc être initiés que par certaines spécialités et certains spécialistes exerçant dans une structure hospitalière ou clinique, mais ils peuvent être renouvelés par les médecins spécialistes libéraux. La PIH devrait être levée en 2024 pour les biomédicaments.
![]() La prescription d'un traitement ciblé est toujours réalisée suite à un bilan préthérapeutique complet pour vérifier l'absence de comorbidités et rechercher d'éventuels facteurs de risque de complications infectieuses. Il va être adapté au traitement choisi car chaque mode d'action a des spécificités sur le plan des effets indésirables. Cependant, certains éléments du bilan préthérapeutique sont communs à toutes les molécules.
La prescription d'un traitement ciblé est toujours réalisée suite à un bilan préthérapeutique complet pour vérifier l'absence de comorbidités et rechercher d'éventuels facteurs de risque de complications infectieuses. Il va être adapté au traitement choisi car chaque mode d'action a des spécificités sur le plan des effets indésirables. Cependant, certains éléments du bilan préthérapeutique sont communs à toutes les molécules.
Interrogatoire
Examen clinique
Examens paracliniques
![]() Le rapport efficacité-tolérance reste toujours positif avec plus de vingt ans de recul pour les plus anciennes biothérapies.
Le rapport efficacité-tolérance reste toujours positif avec plus de vingt ans de recul pour les plus anciennes biothérapies.
Les traitements ciblés sont très efficaces sur les signes inflammatoires cliniques (articulations douloureuses et gonflées), biologiques (CRP voire la VS) et limitent la destruction articulaire en particulier dans la PR et le rhumatisme psoriasique. Leur efficacité anti-inflammatoire permet également de diminuer les risques liés à l'inflammation chronique comme la survenue d'événements cardiovasculaires ou encore d'une ostéoporose. Ils permettent en outre une épargne cortisonique et limitent donc tous les effets iatrogènes inhérents à la corticothérapie.
![]() La tolérance des traitements biologiques et ciblés est en générale bonne. Toutefois, elle peut être pondérée par plusieurs points :
La tolérance des traitements biologiques et ciblés est en générale bonne. Toutefois, elle peut être pondérée par plusieurs points :
La surveillance clinique sera réalisée au cours de consultations de suivi auprès du rhumatologue.
![]() En plus de l'évaluation de l'efficacité, elle est principalement centrée sur la recherche d'éléments en faveur d'une infection présente ou passée. Les infections les plus fréquentes concernent les voies aériennes supérieures, les poumons, la peau et les voies urinaires. Des infections opportunistes comme la tuberculose peuvent débuter par un amaigrissement ou une fébricule.
En plus de l'évaluation de l'efficacité, elle est principalement centrée sur la recherche d'éléments en faveur d'une infection présente ou passée. Les infections les plus fréquentes concernent les voies aériennes supérieures, les poumons, la peau et les voies urinaires. Des infections opportunistes comme la tuberculose peuvent débuter par un amaigrissement ou une fébricule.
![]() La surveillance biologique est simple et comporte à 3 mois de l'initiation du traitement ciblé : une CRP (voire la VS) pour vérifier l'efficacité et un hémogramme, des transaminases, une créatinine pour vérifier la tolérance. Il faudra également un bilan lipidique en cas de traitement par anti-IL-6R et les inhibiteurs de JAK. Cette surveillance est à renouveler ensuite tous les trimestres.
La surveillance biologique est simple et comporte à 3 mois de l'initiation du traitement ciblé : une CRP (voire la VS) pour vérifier l'efficacité et un hémogramme, des transaminases, une créatinine pour vérifier la tolérance. Il faudra également un bilan lipidique en cas de traitement par anti-IL-6R et les inhibiteurs de JAK. Cette surveillance est à renouveler ensuite tous les trimestres.
de fond ciblé biologiques ou synthétiques
![]() Le traitement ciblé doit être arrêté en cas d'infection en dehors de la rhinopharyngite simple (rhume) non surinfectée. Une antibiothérapie sera envisagée en cas d'infection bactérienne après les prélèvements bactériologiques. En cas de signes atypiques et devant toute altération de l'état général, une infection opportuniste doit être évoquée et le patient sera adressé au spécialiste pour un bilan étiologique plus précis.
Le traitement ciblé doit être arrêté en cas d'infection en dehors de la rhinopharyngite simple (rhume) non surinfectée. Une antibiothérapie sera envisagée en cas d'infection bactérienne après les prélèvements bactériologiques. En cas de signes atypiques et devant toute altération de l'état général, une infection opportuniste doit être évoquée et le patient sera adressé au spécialiste pour un bilan étiologique plus précis.
![]() La vaccination du patient et de son entourage est une mesure préventive importante pour réduire le risque infectieux :
La vaccination du patient et de son entourage est une mesure préventive importante pour réduire le risque infectieux :
La majorité des traitements ciblés doivent être transitoirement arrêtés en cas de chirurgie ou de grossesse et il convient d'adresser le patient ou la patiente au spécialiste qui a prescrit le traitement.
Il n'y a aucune contre-indication à voyager quand on est traité par thérapie ciblée ou biomédicament. Il est conseillé d'être en possession d'une information écrite concernant le traitement (nom en DCI, dose et dates) et de respecter les modalités de conservation propre à chaque molécule. Sur place, les mesures d'hygiène et les précautions vis-à-vis de l'alimentation et des insectes doivent être respectées. En cas de fièvre ou de symptômes d'infection, il faut consulter rapidement.
Légende :
Dans le respect de la Réforme du deuxième cycle des études médicales (R2C), les connaissances rassemblées sur ce site sont hiérarchisées en rang A, rang B et rang C à l'aide de balises et d'un code couleur :
![]() Connaissances fondamentales que tout étudiant doit connaître en fin de deuxième cycle.
Connaissances fondamentales que tout étudiant doit connaître en fin de deuxième cycle.
![]() Connaissances essentielles à la pratique mais relevant d'un savoir plus spécialisé que tout interne d'une spécialité doit connaître au premier jour de son DES.
Connaissances essentielles à la pratique mais relevant d'un savoir plus spécialisé que tout interne d'une spécialité doit connaître au premier jour de son DES.
![]() Connaissances spécifiques à un DES donné (troisième cycle).
Connaissances spécifiques à un DES donné (troisième cycle).
